Салон штор в Санкт-Петербурге
Катод это
Катод - это... Что такое Катод?
Катод (от греч. κάθοδος — ход вниз; возвращение) — электрод некоторого прибора, присоединённый к отрицательному полюсу источника тока.
Катод в электрохимии
В электрохимии катод — электрод, на котором происходят реакции восстановления. Например, при электролитическом рафинировании металлов (меди, никеля и пр.) на катоде осаждается очищенный металл.
Катод в вакуумных электронных приборах
В вакуумных электронных приборах катод — электрод, который является источником свободных электронов, обычно вследствие термоэлектронной эмиссии. В электронно-лучевых приборах катод входит в состав электронной пушки.
Катод у полупроводниковых приборов
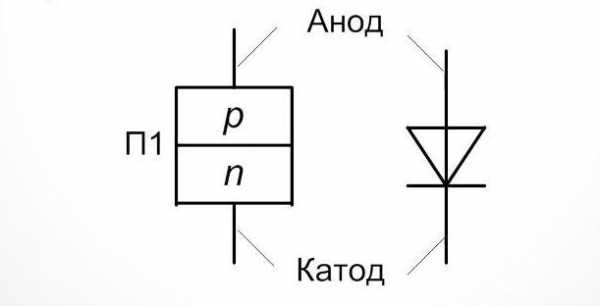
Электрод полупроводникового прибора (диода, тиристора), подключённый к отрицательному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют катодом, подключённый к положительному полюсу — анодом.
Знак анода и катода
В литературе встречается различное обозначение знака катода — «-» или «+», что определяется, в частности, особенностями рассматриваемых процессов.
В электрохимии принято считать, что катод — электрод, на котором происходит процесс восстановления, а анод — тот, где протекает процесс окисления[1][2]. При работе электролизера (например, при рафинировании меди) внешний источник тока обеспечивает на одном из электродов избыток электронов (отрицательный заряд), здесь происходит восстановление металла, это катод. На другом электроде обеспечивается недостаток электронов и окисление металла, это анод.
В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет уже анод. Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод. Так, на приведённой иллюстрации изображён обозначенный знаком «+» катод гальванического элемента, на котором происходит восстановление меди.
В соответствии с таким толкованием, для аккумулятора знак анода и катода меняется в зависимости от направления протекания тока. [2][3][4].
В электротехнике катод — отрицательный электрод, ток течет от анода к катоду, электроны, соответственно, наоборот.
См. также
Литература
- ↑ Антропов Л. И. Теоретическая электрохимия : Учеб. для хим.-технолог. спец. вузов. — 4-е изд., перераб. и доп. — М. : Высш. шк., 1984. — С. 13.
- ↑ 1 2 Лукомский Ю. Я., Гамбург Ю. Д. Физико-химические основы электрохимии: Учебник. — Долгопрудный : Издательский Дом «Интеллект», 2008. — С. 19 — ISBN 978-5-91559-007-5
- ↑ Левин А. И. Теоретические основы электрохимии. — М.: Металлургиздат, 1963. — С. 131.
- ↑ Справочник по электрохимии / Под ред. А. М. Сухотина. — Л. : Химия, 1981. — С. 405.
Ссылки
КАТОД - это... Что такое КАТОД?
катод — а, м. cathode f. <англ. cathode < гр. kathodos путь вниз, спуск. Электрод, соединенный с отрицательным полюсом источника тока (в противоположность аноду). БАС 1. В действии таких приборов, как гальваническая баттарея, полярности нет и быть… … Исторический словарь галлицизмов русского языка
катод — [IEV number 151 13 03] катод Плоская заготовка, получаемая методом электролиза, предназначенная для переплава. [ГОСТ 25501 82] катод Отрицательный электрод рентгеновской трубки [Система неразрушающего контроля. Виды (методы) и технология… … Справочник технического переводчика
КАТОД — (от греч. kathodes ход вниз, возвращение; термин предложен англ. физиком М. Фарадеем в 1834), 1) отрицательный электрод электровакуумного или газоразрядного прибора, служащий источником эл нов, к рые обеспечивают проводимость межэлектродного пр… … Физическая энциклопедия
катод — эмиттер Словарь русских синонимов. катод сущ., кол во синонимов: 4 • термокатод (1) • … Словарь синонимов
КАТОД — КАТОД, электрод, соединенный с отрицательным полюсом батареи. Если в жидкость погрузить две металлические пластины, соединенные с полюсами батареи, то различие между катодом и анодом скажется в следующем: если пластины, из к рых сделаны электроды … Большая медицинская энциклопедия
катод — электровакуумного прибора; катод Электрод, основным назначением которого обычно является испускание электронов при электрическом разряде … Политехнический терминологический толковый словарь
КАТОД — (от греческого kathodos ход вниз, возвращение), электрод электронного либо электротехнического прибора или устройства (например, электровакуумного прибора, гальванического элемента, электролитической ванны), характеризующийся тем, что движение… … Современная энциклопедия
КАТОД — (от греч. kathodos ход вниз возвращение), в широком смысле электрод различных радио и электротехнических устройств или приборов (электронных ламп, гальванических элементов, электролитических ванн и т. д.), характеризующийся тем, что движение… … Большой Энциклопедический словарь
КАТОД — КАТОД, отрицательно заряженный ЭЛЕКТРОД в электролитическом элементе или ЭЛЕКТРОННОЙ ТРУБКЕ. В процессе ЭЛЕКТРОЛИЗА (где электрическая энергия используется для осуществления химических изменений) к нему притягиваются положительно заряженные ионы… … Научно-технический энциклопедический словарь
КАТОД — КАТОД, катода, муж. (греч. kathodos возвращение) (физ.). Отрицательный электрод; ант. анод. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
Анод, катод, положительный и отрицательный: основы химии батарей
04 мая 2020г.
В последнее время были совершены важные открытия в области аккумуляторных батарей (иногда называемых вторичными элементами), и большую часть этой работы можно отнести к разработке электромобилей. Эта работа помогла получить Нобелевскую химическую премию 2019 года за разработку литий-ионных аккумуляторов. Следовательно, термины «анод», «катод», «положительный» и «отрицательный» приобрели все большую важность.
В статьях о новых батарейных электродах и станциях циклирования батарей часто используются названия анод и катод без указания того, разряжается ли батарея или заряжается. Термины анод, катод, положительный и отрицательный не являются синонимами, их иногда можно спутать, что может привести к ошибкам.
Цель этой статьи - прояснить и четко определить эти разные термины.
Реакции окисления и восстановления
Реакция окисления является электрохимической реакцией, которая производит электроны. Электрохимическая реакция, которая происходит на отрицательном элементе цинкового электрода никель-цинковой батареи во время разряда:
Zn + 4OH- → Zn (OH) 2-4 + 2e-
реакция окисления. Окисление - это потеря электронов.
Реакция восстановления - это электрохимическая реакция, которая потребляет электроны. Электрохимическая реакция, происходящая на положительной стороне литий-ионного аккумулятора во время разряда:
Li1 - xCoO2 + XLI++ Xe- → LiCoO2
является реакцией восстановления. Сокращение - это выигрыш электронов.
Анод, катод
- Анод - это электрод, в котором происходит реакция окисления. Потенциал анода, через который протекает ток, выше его равновесного потенциала: Ea (I)> EI = 0 (рис. 1).
- Катод - это электрод, в котором происходит реакция восстановления. Потенциал катода, через который протекает ток, ниже его равновесного потенциала: Ec (I) < EI = 0 (рис. 1).
Рис.1: (EI≠0−EI=0) I > 0
Положительные и отрицательные электроды
Два электрода батареи или аккумулятора имеют разные потенциалы. Электрод с более высоким потенциалом упоминается как положительный, электрод с более низким потенциалом упоминается как отрицательный. Электродвижущая сила, эдс в V батареи - это разность потенциалов положительного и отрицательного электродов, когда батарея не работает.
Исследуя батарею
Разряд батареи
Во время разряда напряжение элемента U, разность между положительным и отрицательным, уменьшается (рис. 2, 3).
- Потенциал положительного электрода E+I≠0 становится меньше его значения в состоянии покоя E+I = 0 : E+I≠0 → положительный электрод является катодом.
- Потенциал отрицательного электрода E-I≠0 становится больше его значения в состоянии покоя E-I=0 : E-I>0 > E-I=0 → отрицательный электрод является анодом.
Рис. 2: Разряд и заряд батареи: слева - потенциальное изменение положительного и отрицательного электродов; справа - изменение напряжения батареи
Зарядка аккумулятора
Во время зарядки напряжение элемента U, разность между положительным и отрицательным, увеличивается (рис. 2, 3).
- Потенциал положительного электрода E+I≠0 становится больше его значения в состоянии покоя E+I=0 : E+I>0 > E+I=0 → положительный электрод является анодом.
- Потенциал отрицательного электрода E-I≠0 становится меньше его значения в состоянии покоя E-I=0 : E-I<0 < E-I=0 → отрицательный электрод является катодом.
Рис. 3: Разрядка / зарядка вторичной батареи, представленной в виде электрохимической ячейки, с электронами и направлением тока.
Вывод
При обычном использовании перезаряжаемой батареи потенциал положительного электрода как при разряде, так и при перезарядке остается больше, чем потенциал отрицательного электрода. С другой стороны, роль каждого электрода переключается во время цикла разрядки / зарядки.
- Во время разряда положительным является катод, отрицательным является анод.
- Во время заряда положительным является анод, отрицательным является катод.
Тексты, описывающие аккумуляторные аноды или катоды, безусловно, косвенно рассматривают случай разряда, что является неполным предсталением о процессах, происходящих внутри вторичного элемента.
Поделиться в соцсетях:
Катод и анод — это плюс или минус: как определить
Анод и катод — два физических термина прикладной электроники, гальванотехнике и химии. Уяснив эти термины, можно понять, почему, например, греется аудиоплеер. Путаница в терминологии спровоцирует аварийные ситуации.
Что это такое
Катоды и аноды — электрические проводники, которые имеют электронную проводимость. Посредством анода электрический заряд втекает в аппаратуру, а катода — наоборот, истекает. На первом возникает окислительная реакция (называют восстановитель) и отсылает заряженные частицы, на втором — восстановительная реакция (называют окислитель) и принимает заряженные частицы.
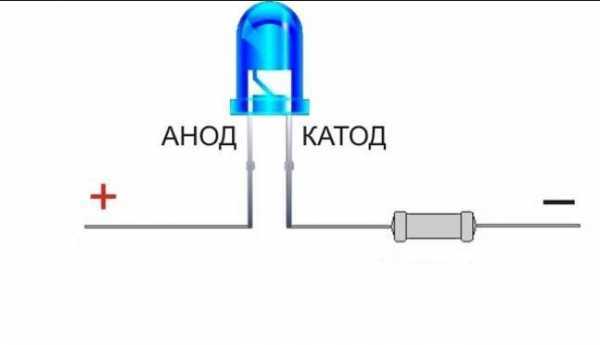 Анод и катод в диоде
Анод и катод в диодеЕсли перемещение электрических проводников проходит от восстановления к окислению по цепи извне, возникает источник электроэнергии. Прибор, с помощью которого преобразовывается химическая энергия в электроэнергию, получил название «гальванический элемент».
Чтобы не возникло путаницы, стоит четко усвоить и запомнить отличие плюса и минуса в разных процессах:
В гальванотехнике химические реакции происходят внутри элемента. В электричестве извне не нуждается, так как заряд сам потечет во внешнюю цепь из элемента. В этом случаев катод — положительный, анод — отрицательный.
 Схема гальванического элемента
Схема гальванического элементаВ электролизе необходим внешний источник тока, включенный в разрыв проводника внешней цепи. Внешний источник создаст разность потенциалов между электрическими проводниками, и вне устройства будет вкачивать ток в элемент. На аноде будет плюс, а на катоде — противоположно.
Важно! Чтобы определить, катод и анод — это плюс или минус, нужно запомнить: в гальванотехнике отрицательным становится анод, а катод — положительный. У электролитов — противоположно.
Как определить что минус, а что плюс (у диода)
Особенность диодов такова, что они проводят заряд только в одном направлении. Чтобы не ошибиться, обычно на корпусе обозначены маркировки. В случае отсутствия маркировок чтобы узнать, как все-таки определить полярности анода и катода у диодов, применяют следующие методы.
- Использование мультиметра. Прибор включается в тест-режим. Если на экране засветились цифровые значения — диод подсоединен по прямому маршруту. Красный провод идет к аноду «+», черный к катоду «-».
- Внешние признаки:
- символы «+» и «-» на корпусе;
- ближе к аноду нанесены обозначения в форме точек или кольцевых линий;
- вытянутая форма устройства — плюс, приплюснутый — минус;
- Включение питания. Собирается простейшая схема, которая состоит из батарейки и лампы.
Обратите внимание! Если включить лампочку, и она начнет гореть — «+» батарейки соединен с положительной полярностью, это есть анод, и прибор будет пропускать через себя ток. Если свет не загорелся, то значит, соединили с отрицательной полярностью — это катод и, соответственно, тока не будет.
- Инструкция по эксплуатации. Производитель вместе с товаром прилагает подробную техническую документацию, где прописаны все необходимые параметры.
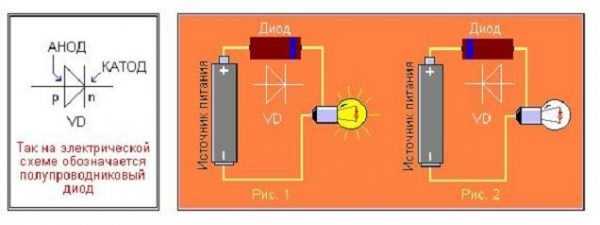 Определение полюсов с помощью лампочки
Определение полюсов с помощью лампочкиЗаряд аккумулятора
Если взглянуть на аккумулятор или обычные батарейки, то можно заметить терминалы, отличающиеся обозначением «+» и «-», которые расположены на противоположных концах.
Аккумулятор имеет металлический или пластиковый каркас. Внутри катод сведен с положительной полярностью, а анод подключен к отрицательной полярности. Отделяет их друг от друга заслон, поэтому они не соприкасаются, а электрический заряд свободно протекает между ними. Помогает этому электролит — специальный раствор серной кислоты.
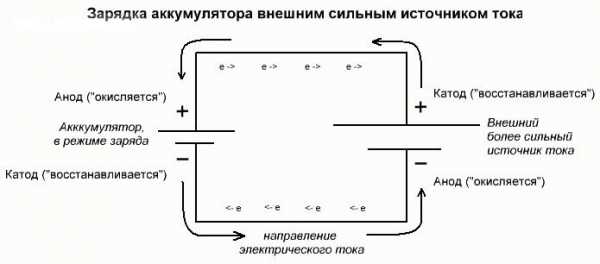 Схема заряда АКБ
Схема заряда АКБКогда проходит химическая реакция заряда с электролитом на одном из электрических проводников, возникнет окислительная реакция. Если включить гальванический компонент в электросеть, электроны с анода перетекут на катод, производя функционирование пока в электролите возникают химические взаимодействия. Работать химический источник электрического тока прекратить только тогда, когда химические составляющие электролита израсходуются.
На заметку. Когда происходит разряд гальванического элемента, то анод является «-», когда заряд — катод имеет знак «+».
Применение в электронике
В электронике применяют особенности диодов впускать заряд по прямому маршруту, но не отпускать обратно.
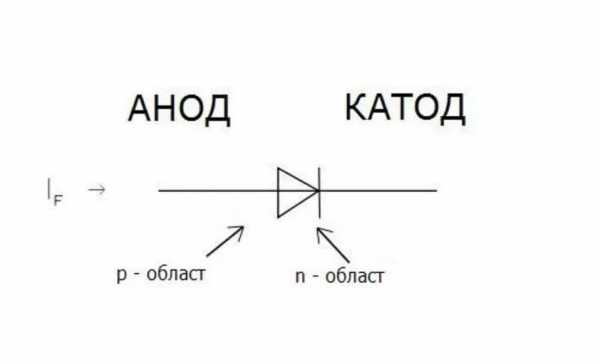 Р-n переход тока
Р-n переход токаРабота светодиода заключается в свойстве кристаллов, которые светятся при пропускании через p-n переход тока по прямой.
В электрохимии электрические проводники необходимы при создании автономных источников питания (аккумуляторные батареи), а также при воспроизведении технологических процессов. Аноды, катоды участвуют в электролизе, электроэкстракции, гальваностегии и гальванопластике.
Гальваника — восстановления металла при химических процессах под воздействием электротока. Такая процедура приводит к устойчивости от коррозии узлов и агрегатов механизмов.
Назначение диода, анод диода, катод диода, как проверить диод мультиметром
Назначение диода - проводить электрический ток только в одном направлении. Когда-то давно применялись ламповые диоды. Но сейчас используются в основном полупроводниковые диоды. В отличие от ламповых они значительно меньше по размеру, не требуют цепей накала и их очень просто соединять различным образом.
Условное обозначение
диода на схеме
На рисунке показано условное обозначение диода на схеме. Буквами А и К соответственно обозначены анод диода и катод диода. Анод диода - это вывод, который подключается к положительному выводу источника питания, непосредственно или через элементы схемы. Катод диода - это вывод из которого выходит ток положительного потенциала и далее через элементы схемы попадает на отрицательный электрод источника тока. Т.е. ток через диод идёт от анода к катоду. А в обратном направлении диод ток не пропускает. Если каким-то из своих выводов диод подключается к источнику переменного напряжения, то на другом его выводе получается постоянное напряжение с полярностью, зависящей от того, как диод подключен. Если он подключен анодом к переменному напряжению, то с катода мы получим положительное напряжение. Если он подключен катодом, то с анода будет получено соответственно отрицательное напряжение.
Как проверить диод мультиметром
Выводы диода
Как проверить диод мультиметром или тестером - такой вопрос встаёт тогда, когда есть подозрение, что диод неисправен. Но, ответ на этот вопрос даёт ещё один ответ, где у диода анод, а где катод. Т.е. если мы изначально не знаем цоколёвку диода, то просто ставим мультиметр или тестер на прозвонку диодов (или на измерение сопротивления) и по очереди прозваниваем диод в обоих направлениях. Если диод исправен, наш прибор будет показывать прохождение тока только в одном из вариантов. Если диод пропускает ток в обоих вариантах - диод пробит. Если он не пропускает ни в каком варианте, диод перегорел и также неисправен. В случае исправного диода, когда он проводит ток, смотрим на клеммы прибора, тот вывод диода, что подключен к положительному выводу тестера, является анодом диода, а тот, что к отрицательному - катодом диода. Проверка диодов очень похожа на проверку транзисторов.
Как выглядит катод. Анод и катод
Любой электровакуумный прибор имеет электрод, предназначенный для испускания (эмиссии) электронов. Этот электрод называется катодом. Электрод, предназначенный для приема эмиттированных катодом электронов, называется анодом.
На анод подают более высокий и положительный относительно катода потенциал.
Катод должен отдавать с единицы поверхности большой ток эмиссии при возможно низкой температуре нагрева и обладать большим сроком службы. Нагрев катода в электровакуумном приборе производится протекающим по нему током.
Такие термоэлектронные катоды разделяются на две основные группы:
- катоды прямого накала,
- катоды косвенного накала (подогревные).
Катоды прямого накала представляют собой металлическую нить, которая непосредственно разогревается током накала и служит для излучения электронов (рис. 6, а ).
Поверхность излучения катодов прямого накала невелика, поэтому от них нельзя получить большой ток эмиссии. Малая теплоемкость нити не позволяет использовать для нагрева переменный ток. Кроме того, при нагреве переменным током температура катода не постоянна во времени, а следовательно, меняется во времени и ток эмиссии.
Положительным свойством катода прямого накала является его экономичность, которая достигается благодаря малому количеству тепла, излучаемого в окружающую среду вследствие малой поверхности катода.
Катоды прямого накала изготовляются из вольфрамовой и никелевой проволоки. Однако большая работа выхода (W 0 = 4,2÷4,5 в) определяет высокую рабочую температуру катода, вследствие чего катод становится неэкономичным. Для повышения экономичности катода вольфрамовую или никелевую проволоку (керн) «активируют» - покрывают пленкой другого элемента. Такие катоды называются активированными.
Если на поверхность керна нанесена электроположительная пленка (пленка из цезия, тория или бария, имеющих меньшую работу выхода, чем материал керна), то происходит поляризация пленки: валентные электроны переходят в керн, и между положительно заряженной пленкой и керном возникает разность потенциалов, ускоряющая движение электрона при выходе его из керна. Работа выхода катода с такой мономолекулярной электроположительной пленкой оказывается меньше работы выхода электрона как из основного металла, так и из металла пленки. При покрытии керна электроотрицательной пленкой, например кислородом, работа выхода катода увеличивается.
Подогревные катоды выполняются в виде никелевых гильз, поверхность которых покрывается активным слоем металла, имеющим малую работу выхода (рис. 6, б ). Внутри катода помещается подогреватель - вольфрамовая нить или спираль, подогрев которой может осуществляться как постоянным, так и переменным током.
Для изоляции подогревателя от гильзы внутренность последней покрывается алундом (Аl 2 O 3).
Подогревные катоды, благодаря их большой тепловой инерции, обычно питают переменным током, значительная поверхность гильзы обеспечивает большой эмиссионный ток. Подогревные катоды, однако, менее экономичны и разогреваются значительно дольше, чем катоды прямого накала.
Параметры и характеристики катодов
Катоды характеризуются следующими основными параметрами:
1. Удельной эмиссией , определяемой величиной тока с одного квадратного сантиметра эмиттирующей поверхности катода при нормальной рабочей температуре.
В электронных лампах с активированными катодами вместо удельной эмиссии часто пользуются параметром,называемым допустимой плотностью катодного тока. Этот параметр характеризуется током, который можно получить с одного квадратного сантиметра поверхности катода при нормальном (рабочем) напряжении накала. Работа при токах с катода, равных току эмиссии в этих лампах, приводит к разрушению поверхности слоя катода.
2. Эффективностью , равной величине тока эмиссии катода, приходящейся на одни ватт затраченной на накал мощности:
Н=I э /P н (12)
где I э - ток эмиссии катода, ма; P н - мощность, затраченная в цепи накала, вт.
3. Сроком службы катода, измеряемым в часах и характеризующим время, в течение которого катод сохраняет необходимые эксплуатационные свойства. Для простых катодов считается, что уменьшение диаметра катода на 10% приводит к его гибели. Соответственно оценивается и срок их службы.
Срок службы активированных катодов определяется уменьшением площади покрытия катода активной пленкой (а следовательно, ухудшением основных параметров лампы) на 20%.
Для выбора оптимального режима работы катода необходимо знать зависимость тока эмиссии катода от его температуры. Непосредственное измерение температуры накаленного катода затруднительно, поэтому пользуются так называемой накальной или эмиссионной характеристикой катода - графически выраженными зависимостями тока накала или тока эмиссии от напряжения или тока накала (рис. 7, а ).
В схеме имеются две цепи: анодная и накальная. Контроль за напряжением накала производится вольтметром V1, непосредственно подключенным в катодную цепь; если необходимо знать ток накала, то в нее включают амперметр. При этом амперметр следует подсоединять к тому зажиму катода, через который проходят накальный и анодный токи в одном направлении: данный конец нити накала нагревается сильнее и работает в наиболее тяжелых тепловых условиях.
Величина тока накала определяется разностью показания амперметра и показания миллиамперметра, но уменьшенного вдвое (так как по этой части цепи проходит примерно половина анодного тока).
Поддерживая постоянным напряжение на аноде, снимают зависимость тока эмиссии от напряжения (или тока) накала. Эмиссионный ток появляется начиная с напряжения на катоде 1-1,5 в и резко возрастает при напряжениях накала, близких к нормальным (рабочим) значениям.
Характеристику I н = ƒ(U н) (см. рис. 7, а ) следует снимать при разомкнутой анодной цепи. Накальная характеристика нелинейна, так как с повышением температуры катода его сопротивление увеличивается. При этом ток накала возрастает меньше, чем увеличивается напряжение накала.
Про анод и катод источника питания необходимо знать тем, кто занимается практической электроникой. Что и как называют? Почему именно так? Будет углублённое рассмотрение темы с точки зрения не только радиолюбительства, но и химии. Наиболее популярное объяснение звучит следующим образом: анод - это положительный электрод, а катод - отрицательный. Увы, это не всегда верно и неполно. Чтобы уметь определить анод и катод, необходимо иметь теоретическую базу и знать, что да как. Давайте рассмотрим это в рамках статьи.
Анод
Обратимся к ГОСТ 15596-82, который занимается химическими Нас интересует информация, размещённая на третьей странице. Согласно ГОСТу, отрицательным электродом является именно анод. Вот так да! А почему именно так? Дело в том, что именно через него электрический ток входит из внешней цепи в сам источник. Как видите, не всё так легко, как кажется на первый взгляд. Можно посоветовать внимательно рассматривать представленные в статье картинки, если содержимое кажется слишком сложным - они помогут понять, что же автор хочет вам донести.
Катод
Обращаемся всё к тому же ГОСТ 15596-82. Положительным электродом химического источника тока является тот, при разряде из которого он выходит во внешнюю цепь. Как видите, данные, содержащиеся в ГОСТ 15596-82, рассматривают ситуацию с другой позиции. Поэтому при консультировании с другими людьми насчет определённых конструкций необходимо быть очень осторожным.
Возникновение терминов
Их ввёл ещё Фарадей в январе 1834 года, чтобы избежать неясности и добиться большей точности. Он предлагал и свой вариант запоминания на примере с Солнцем. Так, у него анод - это восход. Солнце движется вверх (ток входит). Катод - это заход. Солнце движется вниз (ток выходит).
Пример радиолампы и диода
Продолжаем разбираться, что для обозначения чего используется. Допустим, один из данных потребителей энергии у нас имеется в открытом состоянии (в прямом включении). Так, из внешней цепи диода в элемент по аноду входит электрический ток. Но не путайтесь благодаря такому объяснению с направлением электронов. Через катод во внешнюю цепь из используемого элемента выходит электрический ток. Та ситуация, что сложилась сейчас, напоминает случаи, когда люди смотрят на перевёрнутую картину. Если данные обозначения сложные - помните, что разбираться в них таким образом обязательно исключительно химикам. А сейчас давайте сделаем обратное включение. Можно заметить, что полупроводниковые диоды практически не будут проводить ток. Единственное возможное здесь исключение - обратный пробой элементов. А электровакуумные диоды (кенотроны, радиолампы) вообще не будут проводить обратный ток. Поэтому и считается (условно), что он через них не идёт. Поэтому формально выводы анод и катод у диода не выполняют свои функции.
Почему существует путаница?
Специально, чтобы облегчить обучение и практическое применение, было решено, что диодные элементы названия выводов не будут менять зависимо от своей схемы включения, и они будут «прикреплены» к физическим выводам. Но это не относится к аккумуляторам. Так, у полупроводниковых диодов всё зависит от типа проводимости кристалла. В электронных лампах этот вопрос привязан к электроду, который эмитирует электроны в месте расположения нити накала. Конечно, тут есть определённые нюансы: так, через такие как супрессор и стабилитрон, может немного протекать обратный ток, но здесь существует специфика, явно выходящая за рамки статьи.
Разбираемся с электрическим аккумулятором
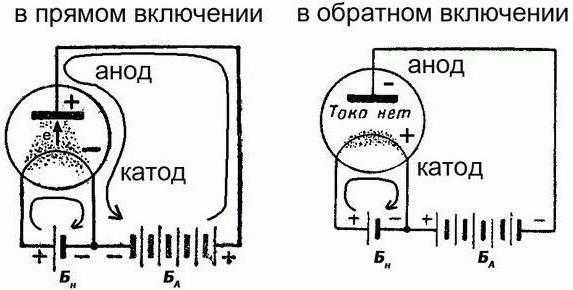
Это по-настоящему классический пример химического источника электрического тока, что является возобновляемым. Аккумулятор пребывает в одном из двух режимов: заряд/разряд. В обоих этих случаях будет разное направление электрического тока. Но обратите внимание, что полярность электродов при этом меняться не будет. И они могут выступать в разных ролях:
- Во время зарядки положительный электрод принимает электрический ток и является анодом, а отрицательный его отпускает и именуется катодом.
- При отсутствии движения о них разговор вести нет смысла.
- Во время разряда положительный электрод отпускает электрический ток и является катодом, а отрицательный принимает и именуется анодом.
Об электрохимии замолвим слово
Здесь используют немного другие определения. Так, анод рассматривается как электрод, где протекают окислительные процессы. И вспоминая школьный курс химии, можете ответить, что происходит в другой части? Электрод, на котором протекают восстановительные процессы, называется катодом. Но здесь нет привязки к электронным приборам. Давайте рассмотрим ценность окислительно-восстановительных реакций для нас:
- Окисление. Происходит процесс отдачи частицей электрона. Нейтральная превращается в положительный ион, а отрицательная нейтрализуется.
- Восстановление. Происходит процесс получения частицей электрона. Положительная превращается в нейтральный ион, а потом в отрицательный при повторении.
- Оба процесса являются взаимосвязанными (так, количество электронов, что отданы, равняется присоединённому их числу).
Также Фарадеем для обозначения были введены названия для элементов, что принимают участие в химических реакциях:
- Катионы. Так называются положительно заряженные ионы, что двигаются в в сторону отрицательного полюса (катода).
- Анионы. Так называются отрицательно заряженные ионы, что двигаются в растворе электролита в сторону положительного полюса (анода).
Как происходят химические реакции?
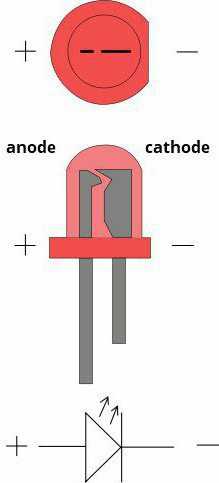
Окислительная и восстановительная полуреакции являются разделёнными в пространстве. Переход электронов между катодом и анодом осуществляется не непосредственно, а благодаря проводнику внешней цепи, на котором создаётся электрический ток. Здесь можно наблюдать взаимное превращение электрической и химической форм энергии. Поэтому для образования внешней цепи системы из проводников разного рода (коими являются электроды в электролите) и необходимо пользоваться металлом. Видите ли, напряжение между анодом и катодом существует, как и один нюанс. И если бы не было элемента, что мешает им напрямую произвести необходимый процесс, то ценность источников химического тока была бы весьма низка. А так, благодаря тому, что заряду необходимо пройтись по той схеме, была собрана и работает техника.
Что есть что: шаг 1
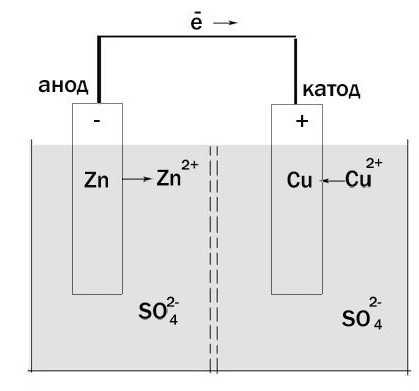
Теперь давайте будем определять, что есть что. Возьмём гальванический элемент Якоби-Даниэля. С одной стороны он состоит из цинкового электрода, который опущен в раствор сульфата цинка. Затем идёт пористая перегородка. И с другой стороны имеется медный электрод, который расположен в растворе Они соприкасаются между собой, но химические особенности и перегородка не дают смешаться.
Шаг 2: Процесс
Происходит окисление цинка, и электроны по внешней цепи двигаются к меди. Так получается, что гальванический элемент имеет анод, заряженный отрицательно, и катод - положительный. Причем данный процесс может протекать только в тех случаях, когда электронам есть куда «идти». Дело в том, что попасть напрямую от электрода к другому мешает наличие «изоляции».
Шаг 3: Электролиз
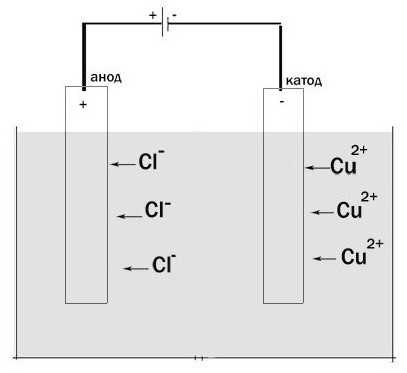
Давайте рассмотрим процесс электролиза. Установка для его прохождения является сосудом, в котором имеется раствор или расплав электролита. В него опущено два электрода. Они подключены к источнику постоянного тока. Анод в этом случае - это электрод, который подключен к положительному полюсу. Здесь происходит окисление. Отрицательно заряженный электрод - это катод. Здесь протекает реакция восстановления.
Шаг 4: Напоследок
Поэтому при оперировании данными понятиями всегда необходимо учитывать, что анод не в 100% случаев используется для обозначения отрицательного электрода. Также катод периодически может лишаться своего положительного заряда. Всё зависит от того, какой процесс на электроде протекает: восстановительный или окислительный.
Заключение
Вот таким всё и является - не очень сложно, но не скажешь, что и просто. Мы рассмотрели гальванический элемент, анод и катод с точки зрения схемы, и сейчас проблем с соединением источников питания с наработками у вас быть не должно. И напоследок нужно оставить ещё немного ценной для вас информации. Всегда приходится учитывать разницу, которую имеет анода. Дело в том, что первый всегда будет немного большим. Это из-за того, что коэффициент полезного действия не работает с показателем в 100 % и часть зарядов рассеивается. Именно из-за этого можно увидеть, что аккумуляторы имеют ограничение на количество раз заряда и разряда.
Изучение таких отраслей, как электрохимия и цветная металлургия, невозможно без понимания в полной мере терминов катод и анод. В то же время эти термины являются неотъемлемой частью вакуумных и полупроводниковых электронных приборов.
Катод и анод в электрохимии
Под электрохимией следует понимать раздел физической химии, изучающий химические процессы, вызываемые воздействием электрического тока, а также электрические явления, вызываемые химическими процессами. Существует два основных вида электрохимических операций:
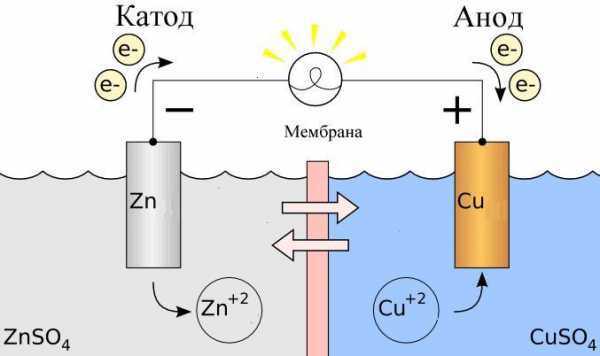
В электрохимии под терминами анод и катод понимают следующее:
- Электрод, на котором проходит окислительная реакция, называется анодом;
- Электрод, на котором осуществляется процедура восстановления, называется катодом.
Под процессами окисления стоит понимать процедуру, при которой частица отдает электроны. Восстановительный процесс подразумевает процедуру принятия электронов частицей. Соответственно, частицы, которые отдают электроны, именуются «восстановителями», и они подвержены окислению. Частицы, которые принимают электроны, именуются «окислителями», они восстанавливаются.
Цветная металлургия широко использует процесс электролиза для выделения металлов из добытых руд и дальнейшей очистки. В процедуре электролиза применяются растворимые и нерастворимые аноды, а сами процессы называются электрорафинированием и электроэкстракцией, соответственно.
Катод в вакуумных приборах
Одной из разновидностей электровакуумных приборов является электронная лампа. Предназначение электроламп – регулирование потока электронов, дрейфующих в вакууме между другими электродами. Конструктивно электролампа выглядит как герметичный сосуд-баллон, с помещенными в середине мелкими металлическими выводами. Численность выводов зависит от вида радиолампы.
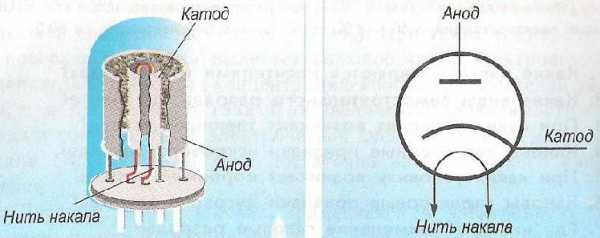
В составе любой радиолампы такие элементы:
- Катод;
- Анод;
- Сетка.
Катодом электролампы подразумевается разогретый электрод, подключенный к «минусу» блока питания и испускающий электроны, будучи накаленным. Эти электроны движутся к аноду, подключенному к «плюсу». Процесс испускания электронов разогретым катодом называется термоэмиссией, а возникший при этом ток именуется током термоэмиссии. Метод нагрева обуславливает разновидности катодов:
- Катод прямого разогрева;
- Катод непрямого разогрева.
Катодом непосредственного накала является прочный вольфрамовый проводник большого сопротивления. Прогревание катода проходит путем подвода к нему напряжения.
Важно! К особенностям электронных ламп непосредственного нагрева относятся быстрый запуск лампы в работу при меньшем потреблении мощности, хотя за счет срока службы. Поскольку питающий ток таких ламп является постоянным, то ограничено их применение в среде переменного тока.
Электролампы, у которых внутри катода, выполненного в виде цилиндра, размещена нагревающая нить, называются радиолампами косвенного нагрева.
Конструктивно анод выглядит в виде пластины либо коробочки, размещенной вокруг катода с сеткой и имеющей потенциал, обратный катоду. Дополнительные электроды, размещенные между анодом и катодом, называются сеткой и применяются для регулировки потока электронов.
Катод у полупроводниковых приборов
К полупроводниковым приборам относятся устройства, состоящие из вещества, удельное электрическое сопротивление которого больше сопротивления проводника, но меньше сопротивления диэлектрика. К особенностям таких приборов относится большая зависимость электропроводимости от концентрации добавок и влияния электрическим током. Свойства p-n перехода определяют принципы работы большей части полупроводниковых компонентов.
Наиболее простым представителем полупроводниковых компонентов является диод. Это элемент, имеющий два вывода и один p-n переход, отличительной особенностью которого выступает протекание тока в одном направлении.
Химические реакции, сопровождающиеся переносом электронов () делятся на два типа: реакции, протекающие самопроизвольно и реакции, протекающие при прохождении тока через раствор или расплав .
Раствор или расплав электролита помещают в специальную емкость — электролитическую ванну .
Электрический ток — это упорядоченное движение заряженных частиц — ионов, электронов и др. под действием внешнего электрического поля. Электрическое поле в растворе или расплаве электролита создают электроды .
Электроды — это, как правило, стержни из материала, проводящего электрический ток. Их помещают в раствор или расплав электролита , и подключают к электрической цепи с источником питания.
При этом отрицательно заряженный электрод катод — притягивает положительно заряженные ионы — катионы . Положительно заряженный электрод (анод ) притягивает отрицательно заряженные частицы (анионы ). Катод выступает в качестве восстановителя, а анод — в качестве окислителя.
Различают электролиз с активными и инертными электродами. Активные (растворимые) электроды подвергаются химическим превращениям в процессе электролиза. Обычно их изготавливают из меди, никеля и других металлов. Инертные (нерастворимые) электроды химическим превращениям не подвергаются. Их изготавливают из неактивных металлов, например, платины , или графита .
Электролиз растворов
Различают электролиз раствора или расплава химического вещества. В растворе присутствует дополнительное химическое вещество — вода , которая может принимать участие в окислительно-восстановительных реакциях.
Катодные процессы
В растворе солей катод притягивает катионы металлов. Катионы металлов могут выступать в качестве окислителей . Окислительные способности ионов металлов различаются. Для оценки окислительно-восстановительных способностей металлов применяют электро-химический ряд напряжений :
Каждый металл характеризуется значением электрохимического потен-циала. Чем меньше потенциал , тем больше восстановительные свойства металла и тем меньше окислительные свойства соответствующего иона этого металла. Разным ионам соответствуют разные значения этого потенциала. Электрохимический потенциал — относительная величина. Электрохимический потенциал водорода принят равным нулю.
Также около катода находятся молекулы воды Н 2 О . В составе воды есть окислитель — ион H + .
При электролизе растворов солей на катоде наблюдаются следующие закономерности:
1. Если металл в соли — активный (до Al 3+ включительно в ряду напряжений ), то вместо металла на катоде восстанавливается (разряжается) водород , т.к. потенциал водорода намного больше. Протекает процесс восстановления молекулярного водорода из воды, при этом образуются ионы OH — , среда возле катода — щелочная:
2H 2 O +2ē → H 2 + 2OH —
Например , при электролизе раствора хлорида натрия на катоде будет вос-станавливаться только водород из воды.
2. Если металл в соли – средней активности (между Al 3+ и Н +) , то на катоде восстанавливается (разряжается ) и металл , и водород , так как потенциал таких металлов сравним с потенциалом водорода:
Me n+ + nē → Me 0
Например , при электролизе раствора сульфата железа (II) на катоде будет восстанавливаться (разряжаться ) и железо, и водород:
Fe 2+ + 2ē → Fe 0
2H + 2 O +2ē → H 2 0 + 2OH —
3. Если металл в соли — неактивный (после водорода в ряду стандартных электрохимических металлов) , то ион такого металла является более сильным окислителем, чем ион водорода, и на катоде восстанавливается только металл:
Me n+ + nē → Me 0
Например, при электролизе раствора сульфата меди (II) на катоде будет восстанавливаться медь:
Cu 2+ + 2ē → Cu 0
4. Если на катод попадают катионы водорода H + , то они и восстанавливаются до молекулярного водорода:
2H + + 2ē → H 2 0
Анодные процессы
Положительно заряженный анод притягивает анионы и молекулы воды. Анод – окислитель. В качестве восстановителей выступаю либо анионы кислотных остаток, либо молекулы воды (за счет кислорода в степени окисления -2: H 2 O -2 ).
При электролизе растворов солей на аноде наблюдаются следующие закономерности:
1. Если на анод попадает бескислородный кислотный остаток , то он окисляется до свободного состояния (до степени окисления 0):
неМе n- – nē = неМе 0
Например : при электролизе раствора хлорида натрия на аноде окисляют-ся хлорид-ионы:
2Cl — – 2ē = Cl 2 0
Действительно, если вспомнить Периодический закон: при увеличении электроотрицательности неметалла его восстановительные свойства уменьшаются . А кислород – второй по величине электроотрицательности элемент. Таким образом, проще окислить практически любой неметалл, а не кислород. Правда, есть одно исключение . Наверное, вы уже догадались. Конечно же, это фтор. Ведь электроотрицательность фтора больше, чем у кислорода. Таким образом, при электролизе растворов фторидов окисляться будут именно молекулы воды, а не фторид-ионы :
2H 2 O -2 – 4ē → O 2 0 + 4H +
2. Если на анод попадает кислородсодержащий кислотный остаток, либо фторид-ион , то окислению подвергается вода с выделением молекулярно-го кислорода:
2H 2 O -2 – 4ē → O 2 0 + 4H +
3. Если на анод попадает гидроксид-ион, то он окисляется и происходит выделение молекулярного кислорода:
4 O -2 H – – 4ē → O 2 0 + 2H 2 O
4. При электролизе растворов солей карбоновых кислот окислению под-вергается атом углерода карбоксильной группы, выделяется углекислый газ и соответствующий алкан.
Например , при электролизе растворов ацетатов выделяется углекислый газ и этан:
2CH 3 C +3 OO – – 2ē → 2C +4 O 2 + CH 3 -CH 3
Суммарные процессы электролиза
Рассмотрим электролиз растворов различных солей.
Например , электролиз раствора сульфата меди . На катоде восстанавли-ваются ионы меди:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются молекулы воды :
Анод (+): 2H 2 O -2 – 4ē → O 2 + 4H +
Сульфат-ионы в процессе не участвуют. Мы их запишем в итоговом урав-нении с ионами водорода в виде серной кислоты:
2 Cu 2+ SO 4 + 2H 2 O -2 → 2Cu 0 + 2H 2 SO 4 + O 2 0
Электролиз раствора хлорида натрия выглядит так:
На катоде восстанавливается водород :
Катод (–):
На аноде окисляются хлорид-ионы :
Анод (+): 2Cl – – 2ē → Cl 2 0
Ионы натрия в процессе электролиза не участвуют. Мы записываем их с гидроксид-анионами в суммарном уравнении электролиза раствора хло-рида натрия :
2H + 2 O +2NaCl – → H 2 0 + 2NaOH + Cl 2 0
Следующий пример карбоната калия.
На катоде восстанавливается водород из воды :
Катод (–): 2H + 2 O +2ē → H 2 0 + 2OH –
На аноде окисляются молекулы воды до молекулярного кислорода :
Анод (+): 2H 2 O -2 – 4ē → O 2 0 + 4H +
Таким образом, при
2H 2 + O -2 → 2H 2 0 + O 2 0
Еще один пример : электролиз водного раствора хлорида меди (II).
На катоде восстанавливается медь :
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются хлорид-ионы до молекулярного хлора :
Анод (+): 2Cl – – 2ē → Cl 2 0
Таким образом, при электролизе раствора карбоната калия ионы калия и карбонат-ионы в процессе не участвуют. Происходит электролиз воды:
Cu 2+ Cl 2 – → Cu 0 + Cl 2 0
Еще несколько примеров: электролиз раствора гидроксида натрия.
На катоде восстанавливается водород из воды :
Катод (–): 2H + 2 O +2ē → H 2 0 + 2OH –
На аноде окисляются гидроксид-ионы до молекулярного кислорода :
Анод (+): 4 O -2 H – – 4ē → O 2 0 + 2H 2 O
Таким образом, при электролизе раствора гидроксида натрия происходит разложение воды, катионы натрия в процессе не участвуют:
2H 2 + O -2 → 2H 2 0 + O 2 0
Электролиз расплавов
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия . На катоде восстанавли-ваются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются анионы хлора :
Анод (+): 2Cl – – 2ē → Cl 2 0
расплава хлорида натрия :
2Na + Cl – → 2Na 0 + Cl 2 0
Еще один пример: электролиз расплава гидроксида натрия . На катоде восстанавливаются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются гидроксид-ионы :
Анод (+): 4OH – – 4ē → O 2 0 + 2H 2 O
Сумарное уравнение электролиза расплава гидроксида натрия :
4Na + OH – → 4Na 0 + O 2 0 + 2H 2 O
Многие металлы получают в промышленности электролизом расплавов.
Например , алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na 3 плавится при более низкой температуре (1100 о С), чем оксид алюминия (2050 о С). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
Al 2 O 3 = Al 3+ + AlO 3 3-
На катоде восстанавливаются катионы алюминия:
Катод (–): Al 3+ + 3ē → Al 0
На аноде окисляются алюминат-ионы :
Анод (+): 4AlO 3 3 – – 12ē → 2Al 2 O 3 + 3O 2 0
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2Al 2 О 3 = 4Al 0 + 3О 2 0
В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C 0 + О 2 0 = C +4 O 2 -2
Электролиз с растворимыми электродами
Если материал электродов выполнен из того же металла, который присут-ствует в растворе в виде соли, или из более активного металла, то на аноде разряжаются не молекулы воды или анионы, а окисляются частицы самого металла в составе электрода.
Например , рассмотрим электролиз раствора сульфата меди (II) с медными электродами.
На катоде разряжаются ионы меди из раствора:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются частицы меди из электрода :
Анод (+): Cu 0 – 2ē → Cu 2+
Среди терминов в электрике встречаются такие понятия как анод и катод. Это касается источников питания, гальваники, химии и физики. Термин встречается также в вакуумной и полупроводниковой электронике. Им обозначают выводы или контакты устройств и каким электрическим знаком они обладают. В этой статье мы расскажем, что это такое анод и катод, а также как определить где они находятся в электролизере, диоде и у батарейки, что из них плюс, а что минус.
Электрохимия и гальваника
В электрохимии есть два основных раздела:
- Гальванические элементы – производство электричества за счет химической реакции. К таким элементам относятся батарейки и аккумуляторы. Их часто называют химическими источниками тока.
- Электролиз – воздействие на химическую реакцию электроэнергией, простыми словами – с помощью источника питания запускается какая-то реакция.
Рассмотрим окислительно-восстановительную реакцию в гальваническом элементе, тогда какие процессы протекают на его электродах?
- Анод – электрод на котором наблюдается окислительная реакция , то есть он отдаёт электроны . Электрод, на котором происходит окислительная реакция – называется восстановителем .
- Катод – электрод на котором протекает восстановительная реакция , то есть он принимает электроны . Электрод, на котором происходит восстановительная реакция – называется окислителем .
Отсюда возникает вопрос – где плюс, а где минус у батарейки? Исходя из определения, у гальванического элемента анод отдаёт электроны .
Важно! В ГОСТ 15596-82 дано официальное определение названий выводов химических источников тока, если кратко, то плюс на катоде, а минус на аноде.
В данном случае рассматривается протекание электрического тока по проводнику внешней цепи от окислителя (катода) к восстановителю (аноду) . Так как электроны в цепи текут от минуса к плюсу, а электрический ток наоборот, тогда катод – это плюс, а анод – это минус.
Внимание: ток всегда втекает в анод!
Или то же самое на схеме:

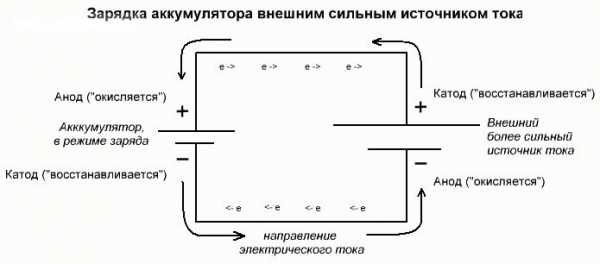
Процесс электролиза или зарядки аккумулятора
Эти процессы похожи и обратны гальваническому элементу, поскольку здесь не энергия поступает за счет химической реакции, а наоборот – химическая реакция происходит за счет внешнего источника электричества.
В этом случае плюс источника питания всё также называется катодом, а минус анодом. Зато контакты заряжаемого гальванического элемента или электроды электролизера уже будут носить противоположные названия, давайте разберемся почему!
Важно! При разряде гальванического элемента анод – минус, катод – плюс, при зарядке наоборот.
Так как ток от плюсового вывода источника питания поступает на плюсовой вывод аккумулятора – последний уже не может быть катодом. Ссылаясь на вышесказанное можно сделать вывод, что в этом случае электроды аккумулятора при зарядке условно меняются местами.
Тогда через электрод заряжаемого гальванического элемента, в который втекает электрический ток, называют анодом. Получается, что при зарядке у аккумулятора плюс становится анодом, а минус катодом.
Процессы осаждения металлов в результате химической реакции под воздействием электрического тока (при электролизе) называют гальванотехникой. Таким образом мир получил посеребренные, золоченные, хромированные или покрытые другими металлами украшения и детали. Этот процесс используют как в декоративных, так и в прикладных целях – для улучшения стойкости к коррозии различных узлов и агрегатов механизмов.
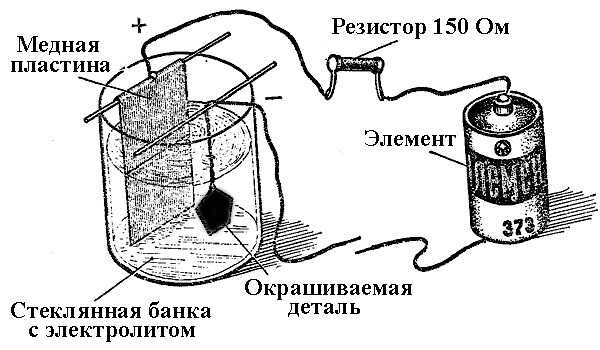
Принцип действия установок для нанесения гальванического покрытия лежит в использовании растворов солей элементов, которыми будут покрывать деталь, в качестве электролита.
В гальванике анод также является электродом, к которому подключаются плюсовой вывод источника питания, соответственно катод в этом случае – это минус. При этом металл осаждается (восстанавливается) на минусовом электроде (реакция восстановления). То есть если вы хотите сделать позолоченное кольцо своими руками – подключите к нему минусовой вывод блока питания и поместите в ёмкость с соответствующим раствором.
В электронике
Электроды или ножки полупроводниковых и вакуумных электронных приборов тоже часто называют анодом и катодом. Рассмотрим условное графическое обозначение полупроводникового диода на схеме:

Как мы видим, анод у диода подключается к плюсу батареи. Он так называется по той же причине – в этот вывод у диода в любом случае втекает ток. На реальном элементе на катоде есть маркировка в виде полосы или точки.
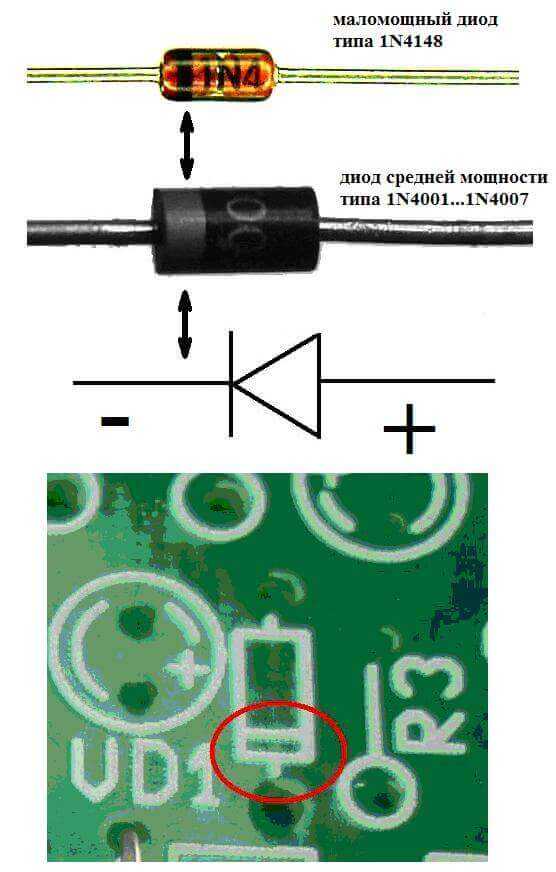
У светодиода аналогично. На 5 мм светодиодах внутренности видны через колбу. Та половина, что больше — это катод.
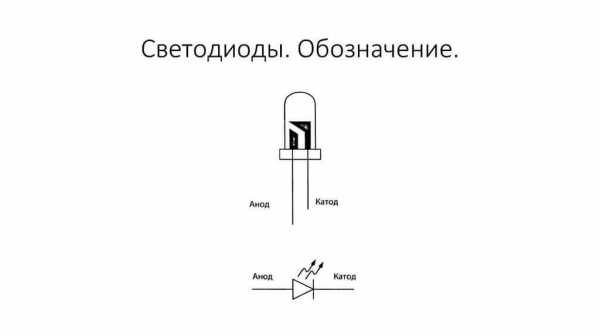
Также обстоит ситуация и с тиристором, назначение выводов и «однополярное» применение этих трёхногих компонентов делают его управляемым диодом:
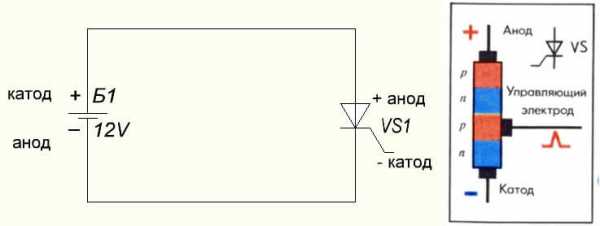
У вакуумного диода анод тоже подключается к плюсу, а катод к минусу, что изображено на схеме ниже. Хотя при приложении обратного напряжения – названия этих элементов не изменятся, несмотря на протекание электрического тока в обратном направлении, пусть и незначительного.
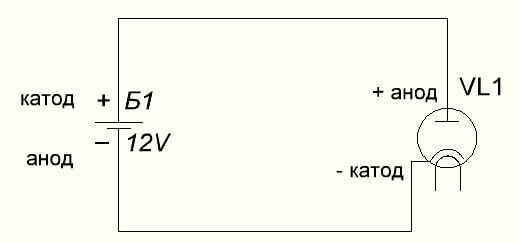
С пассивными элементами, такими как конденсаторы и резисторы дело обстоит иначе. У резистора не выделяют отдельно катод и анод, ток в нём может протекать в любом направлении. Вы можете дать любые названия его выводам, в зависимости от ситуации и рассматриваемой схемы. У обычных неполярных конденсаторов также. Реже такое разделение по названиям контактов наблюдается в электролитических конденсаторах.

Заключение
Итак, подведем итоги, ответив на вопрос: как запомнить где плюс, где минус у катода с анодом? Есть удобное мнемоническое правило для электролиза, заряда аккумуляторов, гальваники и полупроводниковых приборов. У этих слов с аналогичными названиями одинаковое количество букв, что проиллюстрировано ниже:
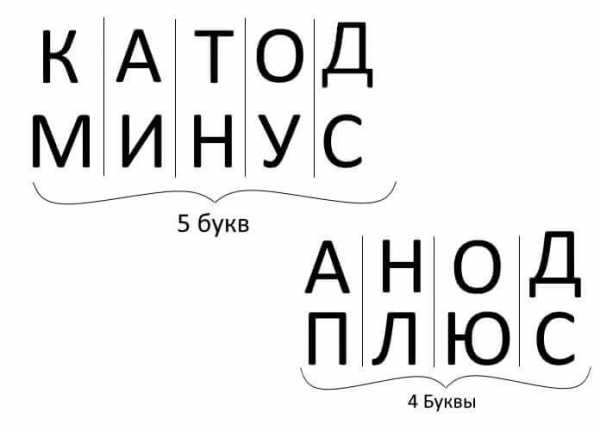
Во всех перечисленных случаях ток вытекает из катода, а втекает в анод.
Пусть вас не собьёт с толку путаница: «почему у аккумулятора катод положительный, а когда его заряжают – он становится отрицательным?». Помните у всех элементов электроники, а также электролизеров и в гальванике – в общем у всех потребителей энергии анодом называют вывод, подключаемый к плюсу. На этом отличия заканчиваются, теперь вам проще разобраться что плюс, что минус между выводами элементов и устройств.
Теперь вы знаете, что такое анод и катод, а также как запомнить их достаточно быстро. Надеемся, предоставленная информация была для вас полезной и интересной!
Материалы
Катоды медные
Назначение и описание
Катоды медные выпускаются по ГОСТ 546, химический состав соответствует ГОСТ 859.
Предназначены для изготовления проволоки, шин, катанки, медных электролитических порошков.
Химический состав
| Элемент | Массовая доля, % | |||
| М1к | М0к | М00к | ||
| Cu | Медь, не менее | 99,95 | 99,97 | –* |
| Примеси, не более: | ||||
| Bi | Висмут | 0,001 | 0,0005 | 0,0003** |
| Sn | Олово | 0,002 | 0,001 | – |
| Ni | Никель | 0,002*** | ||
| Fe | Железо | 0,003 | 0,001 | |
| Zn | Цинк | – | ||
| As | Мышьяк | 0,002 | 0,0005 | |
| P | Фосфор | 0,0015**** | ||
| Sb | Сурьма | 0,0004 | ||
| Pb | Свинец | 0,003 | 0,0005 | |
| Ag | Серебро | 0,002 | 0,002 | |
| S | Cера | 0,004 | 0,0015 | |
| O2 | Кислород | 0,02 | 0,015 | – |
* Знак «–» означает, что данный элемент определяется, но не нормируется.
** Сумма висмута, селена и теллура. Максимальное содержание каждого элемента не должно превышать 0,0002 %.
*** Сумма никеля, цинка, кремния, олова, железа, кобальта.
**** Сумма фосфора, хрома, марганца, мышьяка, кадмия, сурьмы Упаковка и транспортировка
Катоды формируют в пакеты массой не более 1500 кг и высотой не более 500 мм в соответствии с требованиями ГОСТ 21399. Транспортируют всеми видами крытых транспортных средств.
Гарантийный срок хранения
Срок хранения не ограничен.
Качество
Система менеджмента качества АО «Уралэлектромедь» сертифицирована компанией LRQA на соответствие требованиям ISO 9001:2008.
Системы экологического менеджмента, управления охраной труда и промышленной безопасностью, энергетического менеджмента сертифицированы Ассоциацией по сертификации Русский Регистр на соответствие требованиям международных стандартов ISO 14001:2004, OHSAS 18001:2007, ISO 50001:2011.
Катоды медные АО «Уралэлектромедь» зарегистриров
аны на Лондонской бирже металлов: в 2010 г. под брендом UMMC - отделения электролиза ЦЭМ, в 2013 г. под брендом UMMC II - отделения безосновной технологии нового ЦЭМ.
Продукция зарегистрирована в соответствии с европейским регламентом о безопасности химической продукции REACH.
По вопросам приобретения продукции:- Начальник отдела продаж медной продукции ОАО «УГМК» Плотникова Яна Евгеньевна +7 (34368) 9-69-13
Светодиоды (LED) и выпрямители в курсе электроники (2022) »
- Блог
- Статьи
- Основы
- Курс электроники - #6 - кремний и светодиоды (LED)
Пришло время познакомиться на практике со светодиодами, которые можно встретить повсюду.В этой части нашего курса по основам электроники мы проверим на практике работу выпрямительных и светоизлучающих диодов.
В статье рассмотрена самая важная информация, такая как конструкция , классификация, применение диодов и подбор резисторов для светодиодов .
Курс электроники, уровень I (основы) - № 0 - введение, оглавление Курс электроники - № 1 - напряжение, ток, сопротивление и мощность Курс электроники - № 2 - мультиметр, измерения, резисторы Курс электроники - № 3 - Ом и Кирхгоф законы на практике Курс электроники - №4 - конденсаторы, фильтрация питания Курс электроники - №5 - катушки, дроссели Курс электроники - №6 - кремний и светодиоды (LED) Курс электроники - №7а - биполярные транзисторы на практике Курс электроники - №7б - проекты на транзисторах, МОП-транзисторах Курс Курс электроники - №8 - стабилизаторы напряжения Курс электроники - №9 - контактные элементы, реле Курс электроника - №10 - конспект, викторина Вы предпочитаете весь курс в формате PDF (139 страниц)? Закажите электронную книгу и поддержите нашу деятельность » Рекомендуемое продолжение: Курс электроники, уровень II Рекомендуемое продолжение: Курс по основам программирования Arduino Рекомендуемое продолжение: Практический курс пайки Закажи набор элементов и начни учиться на практике! Идти в магазин "Разделение диодов: выпрямительные и осветительные
Как новичок, вам чаще всего будут попадаться два типа светодиодов: выпрямительный и световой (светодиодный) .Вы уже должны почувствовать различия между ними... Одни что-то выпрямляют, а другие светятся. Последним вы будете пользоваться намного охотнее и чаще. Они буквально появятся в 99% ваших электронных проектов.
Внимание! Часто совершается лингвистическая ошибка. Помните, что правильная форма слова «диод» в родительном падеже множественного числа — «диоды»: «В этом проекте я использовал 5 диодов диодов »!
Тип диода (выпрямительный/светоизлучающий) очень легко узнать по внешнему виду элемента.Выпрямительные диоды представляют собой цилиндры различных размеров, через которые аксиально проходит провод. С другой стороны, светящиеся элементы отличаются линзой (прозрачной или цветной) и выводами, которые расположены только с одной стороны элемента. У самых распространенных светодиодов цветной верхний элемент имеет диаметр 5 мм или 3 мм.
Примеры светодиодов показаны на фото ниже. Слева кремниевые диоды, а справа светодиоды.
Слева кремниевые диоды в разных корпусах, справа - светодиоды
Что такое кремниевые (выпрямительные) диоды?
Кремниевые диоды (выпрямители) получили свое название от полупроводникового материала, т.е. кремний .В светоизлучающих диодах функцию полупроводников выполняют другие вещества (об этом позже). У диодов одна основная задача : пропускать ток в одну сторону, а не в другую.
А пока давайте сосредоточимся на знакомстве с основными терминами и символом диода. Обязательно обратите внимание, что распиновка диодов не такая, как у !
Большое значение имеет способ подключения (направление) диода - к счастью, обратное подключение вместо не повредит диод !
Символ диода и корпус образца
Из условного обозначения диода можно вывести принцип его работы: ток течет от анода к катоду , то есть в направлении, указанном «стрелкой» .Ток, протекающий через диод, теряет часть своей энергии, что приводит к снижению напряжения. Проще говоря, если диод является проводящим, на нем есть небольшое падение напряжения (например, 0,7 В), которое мы попытаемся измерить через мгновение.
На практике это означает, что при последовательном включении диода с источником питания напряжение "после диода" будет ниже. Это особенность светодиодов, о которой стоит помнить.
Диод может находиться в двух состояниях: проводимость (когда мы пытаемся заставить ток течь от анода к катоду и диод "на это соглашается", т.е. проводит) и блокировка (когда ток пытается течь от катода к аноду, а диод "не позволяет" и ток не течет).
Диоды - ярлык видео »
Как запомнить, что такое катод и анод?
Постарайтесь запомнить, что катод - это "вывод", к которому следует подключить землю , т.е. минус. Сопоставить легко: в слове "ка т ода" стоит буква т с минусом наверху. Не всем нравятся такие ассоциации, но для многих они являются самым эффективным методом обучения!
Выпрямительный диод на практике
Теперь давайте проведем два эксперимента, которые позволят нам проверить, действительно ли диод проводит только в одном направлении.Нам понадобятся следующие предметы:
- макетная плата,
- Батарея 9В с выводами,
- диоды типа 1N4148,
- Резистор 1 кОм, Мультиметр
- .
можно найти в магазинах (отличаются многими параметрами).В комплекты добавлены диоды популярных 1N4148 , с которыми сталкивался практически каждый электронщик.
Проверим на практике два варианта подключения диода:
90 133Сложные схемы на практике могут выглядеть так:
90 133В первом тесте диод был сделан токопроводящим .Напряжение на его аноде было выше, чем на катоде, поэтому он открылся и пропустил ток примерно 8,9 мА . Во второй попытке диод был вставлен наоборот (напряжение на катоде было выше, чем на аноде), поэтому диод заблокировался и перестал проводить ток - результат - нулевое показание миллиамперметра.
Также стоит измерить, как меняется напряжение в цепи, к которой подключен диод в прямом направлении.Слева показано измерение напряжения от аккумулятора ("перед диодом"), а справа - измерение "за диодом". Как видим, в последнем случае напряжение меньше (по предыдущей информации):
90 133Наиболее важные параметры диодов
Пришло время обсудить основные параметры. На самом деле у диодов гораздо большее количество параметров.Здесь кратко обсуждаются лишь некоторые из наиболее важных.
- Максимальное обратное напряжение. Напряжение, которое можно прикладывать между выводами диода при обратном смещении без риска его повреждения. Более высокое напряжение может сломать диод или даже разрушить его.
Диод, подвергшийся пробою, теряет свои полупроводниковые свойства и проводит ток также в блокировочной конфигурации.
- Максимальный прямой ток. Максимальное значение тока, которое может протекать через диод. Превышение этого значения может разрушить его.
- Максимальная потеря мощности. Диод нагревается во включенном состоянии. Этот нагрев может быть незаметен при малых токах, но при больших токах (200 мА и более) он должен чувствоваться при прикосновении пальца к корпусу. Это связано с тем, что на диод подается определенное напряжение, и через него протекает ток, поэтому излучается мощность. Нельзя допускать, чтобы стоимость этого изделия превышала параметр, указанный в примечании к каталогу, потому что конструкция перегреется и сгорит.Для упомянутого 1N4148 она составляет 0,5 Вт.
-
Прямое напряжение. Напряжение, которое будет между выводами диода при протекании через него тока. Величина этого напряжения зависит от силы протекающего тока.
Предполагается, что кремниевый проводящий диод накапливает на себе ~0,7В.
Однако, как будет показано далее, это не совсем так. При протекании больших токов напряжение может составлять 1-1,2 В .В следующем фрагменте примечания к каталогу для диода 1N4148 (производства NXP) показана диаграмма зависимости между прямым напряжением и прямым током.
Вольт-амперная характеристика диода
Как видно из графика выше, при пропускании тока 100 мА через диод при температуре около 25°С на нем будет осаждаться примерно 0,9 В . Характеристики, указанные в примечаниях к каталогу, следует рассматривать как ориентировочные, поскольку отдельные светодиоды могут отличаться друг от друга.
Измерение прямого напряжения диода
Мультиметрыпозволяют измерять прямое напряжение диода. Счетчик должен быть переключен в положение, отмеченное символом диода. К сожалению, это измерение можно трактовать только как ориентировочное, по принципу: "диод проводит/не проводит", т.к. оно выполняется при неизвестном прямом токе.
После установки измерителя в соответствующее положение производим измерение так же, как и при проверке сопротивления резисторов. Здесь, однако, важна полярность, черный щуп (подключенный к СОМ) нужно приложить к клемме, отмеченной полоской на корпусе диода.
Пример измерения может выглядеть следующим образом:
Измерение прямого напряжения диода
Диод как защита по питанию?
Включение диода последовательно с блоком питания позволяет решить проблему реверсивного питания, т.к. при попытке поменять местами полюса аккумулятора он перейдет в заблокированное состояние и не будет пропускать ток. К сожалению, во время проведения на нем будет некоторое напряжение. Это снижение следует учитывать при выборе источника питания системы.
О вышесказанном забывают многие новички, желающие запитать цифровые схемы перед диодом и использовать источник, дающий 5В.Пройдя через диод, мы получим около 4,3 В, что может быть слишком мало для цифровых схем.
Выпрямительный диод для защиты от обратного питания
Диоды Шоттки
Кроме кремниевых диодов существуют еще т.н. Диоды Шоттки - обычно изготавливаются для более низких напряжений, чем кремниевые диоды (обычно от 20 В до 100 В), но с меньшим падением напряжения в прямом направлении. Однако эти элементы не рассматриваются более подробно в нашем курсе основ электроники.
На этом мы завершаем обсуждение кремниевых диодов. Хотя мы не касались их токового «выпрямляющего» свойства (отсюда и второе название: выпрямительные диоды), в курсе не рассматривается переменный ток, так что выпрямлять здесь нам было бы нечего.
Светодиод - Светодиоды на практике
LED ( светодиод ) - светоизлучающие диоды, реже называемые светодиодами, являются одним из самых важных и интересных элементов.
Пример использования диода и условного обозначения
в схемах
До сих пор мы имели дело с диодами, основной задачей которых было проводить ток только в одном направлении . Между тем, есть столь же многочисленная (если не более многочисленная) группа светодиодов, которые тоже светятся. Они содержат в своей структуре небольшой кристалл вещества, который светится при подаче на него напряжения. Однако точная информация по этому вопросу выходит далеко за рамки основ электроники. Так что тут смотреть не надо.
Сечение диода - осветительный элемент
Светящаяся внутренняя часть диода является полупроводником, т.е. способна блокировать ток, который хотел бы течь в неправильном направлении. Это видно даже по условному обозначению светодиодов.
Следовательно, правильно подключенный диод будет светиться и одновременно через него будет протекать ток. Неправильно подключенный диод будет выключен и блокирует протекание тока.
90 133Запомните раз и навсегда, что для каждого светодиода требуется правильно подобранный резистор ! Отсутствие резистора означает, что в цепи протекает слишком большой ток, который сжигает диод — через мгновение вы узнаете, как выбрать такой резистор.
Отсутствие резистора и слишком большой ток повредят диод
.Как идентифицировать светодиодные выходы?
Светоизлучающие диоды (СИД) не имеют черных полос на корпусе. Однако отличить катод (или минус) можно еще несколькими способами. Идем по порядку самого популярного варианта:
- в новом катоде диода самый короткий вывод,
- край линзы диода рядом с катодом обрезан, Катод
- соединяется с «большой пластиной» в корпусе диода.
Характеристика элементов диода
Эти методы хорошо работают для 99,99% светодиодов. Однако вам могут попадаться какие-то странные, "китайские" светодиоды или старые элементы с разборки, у которых вся маркировка будет указывать на противоположный вывод - такие случаи не легенда, они уже описывались на нашем форуме!
В таких ситуациях единственным верным методом является подключение диода через резистор к источнику питания или измерение мультиметром в режиме измерения диода.
Существуют также диоды, которые имеют несколько световых структур в одном корпусе. Благодаря этому удается получить множество нестандартных цветов. Подробнее о таких диодах вы узнаете, если решите выполнить упражнения из курса электроники, уровень II :
Параметры светодиодов
Светодиоды характеризуются теми же параметрами, что и выпрямительные диоды, но больше внимания уделяется другим из этих характеристик (например, цвету, яркости, углу луча).Наиболее важным, однако, является прямой ток . Для диодов типа входящих в комплект максимальный прямой ток около 20 мА. Однако современные светодиоды очень ярко светят даже при токе 1-2 мА. Поэтому этот ток обычно ограничивается очень малыми значениями.
Максимальное обратное напряжение обычно 5-6В, поэтому будьте осторожны при подключении диода к более высокому источнику питания, так как может повредить его .
Прямое напряжение сильно зависит от цвета светодиода. Каждый цвет получается из разных веществ с разными электрическими свойствами. Подробную информацию по этому вопросу можно найти в документации на диоды. Однако для целей хобби DIY можно взять и примерные значения из нашей таблицы:
Должны ли светодиоды иметь цветную линзу? Нет, свет создается материалом, из которого изготовлен диод. Часто можно встретить цветные светодиоды в прозрачных корпусах.Особенно это касается так называемого яркие светодиоды, т.е. те, которые дают очень сильный свет.
Светоизлучающие диоды (LED) - видеоотчет »
Согласование резистора со светодиодом (LED)
Диоды должны быть ограничены по току. Самое простое решение - вставить резистор последовательно со светодиодом. По закону Кирхгофа часть напряжения пойдет на диод, а остальное - на резистор.Более того, зная (более-менее) напряжение, которое «примет» резистор, можно — по закону Ома — рассчитать ток, протекающий через него. Эти элементы соединены последовательно, поэтому через диод будет течь один и тот же ток, что нас в основном и интересует.
Формула для расчета сопротивления резистора для питания светодиода выглядит следующим образом:
- U и - напряжение питания для схемы с диодом
- U диоды - диоды прямого напряжения (из таблицы выше)
- I диоды - ток протекающий через диод
Принципиальная схема подключения светодиодного диода к блоку питания
Рассчитаем номинал резистора в системе с питанием от 9 В.Предположим, прямое напряжение диода составляет 2 вольта, и вы хотите, чтобы через него проходило 7 мА. Пишем значения:
- U и = 9 В
- У диоды = 2В Диоды
- и = 7 мА = 0,007 А
Рассчитываем номинал необходимого резистора:
R = (9 В - 2 В) / 0,007 А = 7 В / 0,007 А = 1000 Ом = 1 кОм
Сейчас мы проверим такую систему на практике!
Какой ток должен протекать через диод? Определенно меньше максимального, т.е. уже заданного 20 мА.Выпускаемые сегодня светодиоды достаточно яркие, когда через них протекает ток <10 мА. В системах с батарейным питанием, где важно низкое энергопотребление, можно использовать 1–5 мА.
Слишком низкий ток проводимости не повредит диод, а только ослабит его световую мощность.
Светодиод загорается в зависимости от выбранного резистора
Стандартно для напряжения питания 5 В и прямого напряжения 2 В используются резисторы 330 Ом . Это заставляет около 9 мА протекать через диод.В комплект входит батарейка с напряжением 9 В. С красным диодом, на который нужно около 2 В, на резистор будет подано напряжение 7 В. С помощью резистора 1 кОм через него будет протекать ток около 7 мА диод - так что этот выбор будет очень удачным (такой пример рассматривался выше для расчетов).
Теперь проверим эту систему на практике:
В качестве эксперимента проверьте, как поведет себя диод при еще большем уменьшении его тока. Для проверки можно использовать потенциометр, который, в конце концов, является регулируемым резистором.Соедините его последовательно с резистором 330 Ом так, чтобы в момент малейшего поворота потенциометра последовательно было хотя бы это маленькое сопротивление.
Потенциометр в одном положении будет иметь сопротивление ~0 Ом, поэтому ничто не будет ограничивать ток, протекающий через диод, что приведет к его повреждению. Дополнительный резистор защитит его от подгорания.
90 133Яркость диода должна изменяться в зависимости от текущей настройки потенциометра.Для теста также стоит заменить диод на копию другого цвета.
Должен ли резистор находиться перед диодом?
Многие новички считают, что резистор должен быть физически «перед» диодом, иначе слишком большой ток повредит его. К счастью, это не так — помните, что порядок элементов в этой комбинации вообще не имеет значения . По последовательно соединенным элементам течет один и тот же ток — это следует из рассмотренных ранее законов Кирхгофа.
90 133Эта тема довольно "спорная" для многих новичков, которые часто не могут в ней разобраться.Поэтому мы подготовили отдельную дополнительную статью , разъясняющую только этот, но крайне важный вопрос. Обязательно прочтите:
Как запитать несколько светодиодов?
Если мы хотим запитать несколько светодиодов от одного источника, мы можем использовать одно из двух решений:
- Каждый диод можно снабдить своим резистором, рассчитанным по заранее выбранным рекомендациям, а затем такую серию (диод + резистор) подключить параллельно к источнику питания.
- Можно еще соединить несколько диодов последовательно и подобрать к нему резистор. Тогда напряжение U диода в формуле надо брать столько раз, сколько диодов. Напряжение питания U и должно быть хотя бы на несколько вольт выше предполагаемого U диода .
Не следует подключать одинаковые светодиоды параллельно, даже если они одного цвета! Прямое напряжение для каждого из них будет немного отличаться, поэтому некоторые будут светиться тускло, а некоторые могут быть повреждены, потому что через них будет протекать большая часть тока.
Теперь для теста подключите несколько светодиодов в соответствии с первым предложенным решением. Однако помните, что у каждого светодиода есть свой резистор — иначе можно повредить схему! Пример схемы:
90 133Достаточно нескольких элементов, чтобы получить действительно интересный эффект:
Различные цвета светодиодов на практике
Действительно стоит запомнить формулу, приведенную в этой части руководства, и научиться выбирать резистор.Мы знаем, что многие люди борются с этим. Поэтому мы подготовили отдельную статью, в которой затронута только эта тема. В нем можно найти и более замысловатые примеры:
Домашнее задание
Сравните яркость диодов разных цветов. Какой диод лучше светит при слабом токе, а какой хуже? Эксперимент следует повторить в светлой и темной обстановке.
Время викторины - проверьте, что вы уже знаете!
Вы уже прошли шесть разделов курса, поэтому смело приступайте к следующему тесту, который состоит из 15 тестовых вопросов (один вариант ответа), ограничение по времени 15 минут.Учитывается первый результат, но позже вы сможете пройти тест несколько раз (в рамках обучения).
Перейти к викторине №2 из 4 »
Без стресса! старайтесь отвечать на вопросы как знаете, используйте свои записи в случае возникновения проблем. Это не гонки — эта викторина поможет закрепить уже полученные знания и уловить возможные темы, которые стоит повторить. Удачи!
Последние результаты викторины
Вот результаты 10 человек, которые недавно прошли викторину. Теперь пришло время для вас! Примечание. Записи в этой таблице могут быть задержаны, полные результаты доступны на этой странице теста.
| # | Пользователь | Дата | Результат |
|---|---|---|---|
| 1 | камиксель | 30.04.2022, 13:49 | 100%, за 196 сек. |
| 2 | кружка мал | 30.04.2022, 20:23 90 535 90 534 93%, за 127 сек. 90 535 90 531 90 522 90 534 3 90 535 90 534 godlewski99 90 535 90 534 1 мая 2022 г., 22:50 90 535 90 534 93%, за 133 сек. | |
| 4 | LukaszSPSJ | 01.05.2022, 12:58 | 93%, за 189 сек. |
| 5 | Pitt90 | 01.05.2022, 12:04 | 93%, за 192 сек. |
| 6 | AdrianJaw | 1 мая 2022, 21:00 90 535 90 534 93%, за 201 сек. | |
| 7 | Викус | 30.04.2022, 18:00 90 535 90 534 93%, через 222 сек. 90 535 90 531 90 522 90 534 8 90 535 90 534 Алексей 90 535 90 534 1 мая 2022, 00:12 90 535 90 534 80%, за 123 сек. 90 535 90 531 90 522 90 534 9 90 535 90 534 лоурнек 90 535 90 534 2 мая 2022, 16:49 90 535 90 534 73%, за 103 сек. | |
| 10 | DrKondziu | 2 мая 2022, 23:03 90 535 90 534 73%, за 243 сек. |
Резюме
Несколько практических советов по светодиодам. Вы узнали об их основных параметрах и областях применения.О светодиодах можно написать очень толстую книгу, и она все равно не исчерпает тему. Пожалуйста, рассматривайте эту статью как введение в этот вопрос. В случае возникновения проблем, не стесняйтесь спрашивать в комментариях. Также нам будет очень приятно, если вы поделитесь результатами своих экспериментов и напишите, все ли прошло гладко!
Самое главное после этого урока уметь подобрать подходящие резисторы для питания светодиода . Вы будете сталкиваться с выученными частями много раз. Светодиоды – самый популярный элемент, позволяющий сигнализировать о происходящем в системе.
Показать/скрыть все части Курс электроники, уровень I (основы) - № 0 - введение, оглавление Курс электроники - № 1 - напряжение, ток, сопротивление и мощность Курс электроники - № 2 - мультиметр, измерения, резисторы Курс электроники - № 3 - Ом и Кирхгоф законы на практике Курс электроники - №4 - конденсаторы, фильтрация питания Курс электроники - №5 - катушки, дроссели Курс электроники - №6 - кремний и светодиоды (LED) Курс электроники - №7а - биполярные транзисторы на практике Курс электроники - №7б - проекты на транзисторах, МОП-транзисторах Курс Курс электроники - №8 - стабилизаторы напряжения Курс электроники - №9 - контактные элементы, реле Курс электроника - №10 - конспект, викторина Вы предпочитаете весь курс в формате PDF (139 страниц)? Закажите электронную книгу и поддержите нашу деятельность » Рекомендуемое продолжение: Курс электроники, уровень II Рекомендуемое продолжение: Курс по основам программирования Arduino Рекомендуемое продолжение: Практический курс пайки Закажи набор элементов и начни учиться на практике! Идти в магазин "PS Если вы готовы к этому, вы можете постепенно начать читать наш курс программирования Arduino - это, несомненно, станет следующим шагом в вашем электронном образовании!
Текущая версия курса: Дамиан Шимански, иллюстрации: Петр Адамчик.P первая версия: Михал Куржела. Схемы сборки выполнены с частичным использованием программного обеспечения Fritzing (и собственных библиотек компонентов). Запрещение копирования содержания курса и графики без согласия FORBOT.pl
Дата последней проверки или обновления этой записи: 13.04.2022 .
Статья была интересной?
Присоединяйтесь к 11 000 человек, которые получают уведомления о новых статьях! Зарегистрируйтесь и вы получите файлы PDF с (м.в по питанию, транзисторам, диодам и схемам) и список вдохновляющих DIY на основе Arduino и Raspberry Pi.
диоды кремниевые, курс Электроника, светодиоды, полупроводники, светящиеся, блокирующие
.• Электроды, сварочные прутки, электроды, сварочные прутки • domero.pl
Электрод - элемент, замыкающий некоторые электрические системы или устройства. Электроды предназначены для отправки или получения электрического заряда или для создания вокруг них электростатического поля. Электроды бывают трех видов: катод , анод, сетки в трубке . Электроды подразделяются по оболочке, размеру, весу, упаковке...
Электрод - элемент, замыкающий некоторые электрические системы или устройства. Электроды предназначены для отправки или получения электрического заряда или для создания вокруг них электростатического поля. Электроды бывают трех видов: катод , анод, сетки в трубке . Электроды делятся по покрытию, размеру и весу упаковки.
Катод
Катод Предназначен для отправки отрицательного заряда или приема положительного . И электроны, и ионы могут быть зарядами, протекающими через катод.В устройствах, вырабатывающих электричество, катод является положительным электродом по отношению к аноду. С другой стороны, в устройствах, которые получают электрический ток, катод отрицателен к аноду .
Анод
Анод предназначен для отправки положительного заряда или приема отрицательного , все делается в устройствах замкнутого цикла на постоянном токе. Через анод могут протекать как электроны, так и ионы. В устройствах, генерирующих электрический ток, анод является отрицательным электродом катода.
Крышка
Крышка адаптирована к условиям сварки, поэтому можно различить множество типов крышек . Покрытие изготавливается из различных смесей металлов, минеральных соединений и материалов, образующих защитный слой. В основном химический состав футеровки отличается, другой химический состав футеровки приведет к разному химическому составу соединений.Покрытие должно обогатить химический состав сварного шва, чтобы сделать сварной шов более прочным. Он также защищает стык от попадания воздуха и различной пыли, загрязняющей стык.
Размеры электродов
Существует несколько основных размеров электродов: 1,6, 2,0, 2,5, 3,25, 4,0, 5,0, 6,0, это размеры диаметра электрода в мм. Однако длины электродов находятся в следующих диапазонах: 250, 300, 350, 400, 450, все размеры даны в мм.
| ♦ METALWELD НОВЫЙ ЭЛЕКТРОД С ДВОЙНЫМ ПОКРЫТИЕМ ♦ DOMERO.PL |
 |
Основные города, в которые мы посылаем наши продукты:
• Białystok, • Bydgoszzz, • ronzne, • rzzń • , • Щецин, • Варшава, • Вроцлав, • Зелена-Гура.
.База Знаний: INR, ICR И CAN NCA - КОНСТРУКЦИЯ И ХИМИЯ ЛИТИЙ-ИОННЫХ АККУМУЛЯТОРОВ - BatLit
В статье, посвященной базовым знаниям о Li-Ion аккумуляторах, вы узнали, из чего состоят отдельные элементы. Теперь углубимся в эту тему еще больше - посмотрим, из чего сделаны отдельные элементы аккумуляторов 18650 и как это влияет на их характеристики и работу.
Li-Ion аккумуляторы состоят из 4 основных элементов:
- сепаратор - пористая фольга (полиолефиновая мембрана), защищающая от прямого контакта электродов (короткого замыкания), но допускающая перенос ионов лития Электролит
- - смесь органических растворителей (пропиленкарбонат, этиленкарбонат, гликоли, органические эфиры), в которых растворены химически сложные соли лития (LiPF6, LiBF4, LiCIO4, LiCF3SO3).Электролит может быть в виде жидкости или твердого вещества в виде проводящих полимеров, содержащих соли лития (LiPo). Благодаря электролиту ионы лития могут перемещаться между электродами
- отрицательный электрод (анод) из пористого углерода, например графита
- положительный электрод (катод) из соединений лития
Первые 3 элемента существенно не различаются между разными моделями литий-ионных аккумуляторов. Однако последний компонент — катод — это элемент, химический состав которого определяет характеристики данного литиевого элемента: нагрузочную способность, емкость, количество циклов и безопасность.
В таблице ниже приведены наиболее популярные химические составы катодов аккумуляторов 18650:
оксид марганца лития KATODA/IMR/LMO
Структура оксида, содержащегося в этом катоде, улучшает поток ионов лития, что приводит к низкому внутреннему сопротивлению и, следовательно, к высокой эффективности тока батареи. Отличительная конструкция позволяет увеличить соответствующую одну из трех характеристик (за счет двух других): срок службы, производительность или емкость.Дополнительным преимуществом является термическая стабильность и повышенная безопасность. Низкое внутреннее сопротивление обеспечивает быструю зарядку и разрядку высоким током. Ячейки IMR 18650 могут «пожертвовать» 20-30А при относительно небольшом повышении температуры. Некоторые аккумуляторные батареи можно заряжать импульсным (1 сек.) током до 50А. Однако разряд такого постоянного тока большой силы вызвал бы значительное повышение температуры, даже выше допустимых 80°С. Недостатком таких аккумуляторов является относительно небольшое количество циклов - 300-700.Хотя элементы IMR не очень популярны, они все еще используются в электроинструментах, медицинском оборудовании, а также в электрических и гибридных транспортных средствах.
оксид кобальта марганца никеля лития КАТОДА/ИНР/НМК
Одним из лучших сочетаний в конструкции катода является никель, марганец и кобальт. Структура этого оксида, подобная ЖМО, позволяет создать элемент с повышенной емкостью, выходом по току или сроком службы. Секрет успеха элементов NMC заключается в сочетании никеля и марганца.Самым большим преимуществом никеля является накопление энергии, но сам по себе он не очень стабилен. С другой стороны, марганец, благодаря упомянутой выше характерной структуре, снижает внутреннее сопротивление. К сожалению, он плохо накапливает энергию сам по себе. Эти два металла, однако, объединенные в одном соединении, прекрасно дополняют друг друга и подчеркивают их преимущества. Сила этих аккумуляторов также заключается в количестве циклов, которое варьируется от 1000 до 2000 циклов.
литий-никель-кобальт-глинозем KATODA/NCA
Структура этого катода аналогична структуре NMC, за исключением того, что марганец заменен алюминием.В результате текущая эффективность ячеек NCA относительно низка. Тем не менее, эти батареи компенсируют свою высокую емкость и долговечность. Благодаря исключительной долговечности их часто можно встретить в электромобилях, в том числе в автомобилях Tesla. Эти элементы имеют длительный срок службы, поэтому могут храниться длительное время без потери емкости, но, к сожалению, имеют очень низкое количество рабочих циклов, т.к. всего около 500.
Окись кобальта лития KATODA/ICR/LCO
LCO был первым катодом из оксида металла, добившимся коммерческого успеха.Эта химия позволяет запасать большое количество энергии, следовательно они могут быть очень емкими, к сожалению за счет сравнительно небольшого срока службы, количества циклов (500-1000), термостабильности и выхода по току. Максимальный зарядный и разрядный ток в батареях ICR не превышает 1С. Например, аккумулятор емкостью 3,5Ач будет иметь ток не более 3,5А. Следовательно, эти ячейки идеально необходимы в таких устройствах, как камеры, ноутбуки и фотоаппараты.
<< НАЗАД
ПРОЧИЕ ИЗДЕЛИЯ:
ЧТО НА САМОМ ДЕЛЕ ЭТО LI-ION
ПРИМЕНЕНИЕ ЛИТИЙ-ИОННЫХ АККУМУЛЯТОРОВ
ПРЕИМУЩЕСТВА И НЕДОСТАТКИ ЛИТИЙ-ИОННЫХ АККУМУЛЯТОРОВ
LI-ION - СОВЕТЫ И ПРИМЕНЕНИЕ
LI-ION
ТЕСТИРОВАНИЕ ЕМКОСТИ АККУМУЛЯТОРАСДЕЛАЙ САМ - МЫ СОЗДАЕМ LI-ION АККУМУЛЯТОР
.Катод G015Y O2 с серебряным сердечником - 11.848.231.350 - Kjellberg / Машинная резка
Настройки файлов cookie
Здесь вы можете определить свои предпочтения в отношении использования нами файлов cookie.Требуется для работы страницы
Эти файлы cookie необходимы для работы нашего веб-сайта, поэтому вы не можете их отключить.
Функциональный
Эти файлы позволяют использовать другие функции сайта (кроме необходимых для его работы).Включив их, вы получите доступ ко всем функциям веб-сайта.
Аналитический
Эти файлы позволяют нам анализировать наш интернет-магазин, что может способствовать его лучшему функционированию и адаптации к потребностям Пользователей.
Поставщики аналитического программного обеспечения
Эти файлы используются поставщиком программного обеспечения, под которым работает наш магазин.Они не объединяются с другими данными, введенными вами в магазине. Целью сбора этих файлов является выполнение анализа, который будет способствовать разработке программного обеспечения. Вы можете прочитать больше об этом в политике использования файлов cookie Shoper.
Маркетинг
Благодаря этим файлам мы можем проводить маркетинговые мероприятия.
.Как работает магниевый анод? | Строим Дом
Ответ эксперта: Защитные аноды в резервуарах для хранения горячей воды чаще всего они содержат магний. Это металл, который легко вступает в химические реакции, поэтому в первую очередь он реагирует с кислородом и различными веществами в воде, а не со сталью, из которой сделан бак. Магниевый анод изнашивается - чем быстрее, тем агрессивнее свойства воды.
Чаще всего мы имеем дело с так называемыми электрохимическая коррозия, представляющая собой реакцию между двумя металлами, связанными вместе электролитом – электропроводящей жидкостью. Обычная вода является электролитом, потому что она никогда не бывает химически чистой. В результате так называемая гальванический элемент. Атомы магния отдают электроны и переходят в раствор в виде положительно заряженных ионов. Этот менее благородный металл вытесняет из раствора второй, менее реакционноспособный металл, то есть железо.
Электрохимическая серия - что это такое?
Реактивность графически может быть представлена так называемымэлектрохимический ряд. Чем более отрицателен потенциал металла по отношению к водороду, тем он менее благороден и тем легче распадается на электроны и положительные ионы. С другой стороны, положительный потенциал характеризует более благородные металлы с меньшей реакционной способностью.
Вот несколько примеров из электрохимического ряда:
- золото +1,42 В;
- серебро +0,80 В;
- медь +034 В;
- вывод -0,12 В; железо
- -0,44 В;
- магний -2,44В
Как видно из списка, у магния потенциал на целых -2 В ниже, чем у железа, являющегося основным компонентом стали. Бак ГВС и представляет собой гальванический элемент, где один полюс (катод) — это сам стальной бак, другой — магниевый анод, а электролит — водопроводная вода. В этой системе разрушается (отдает электроны и ионы раствору) более реактивный магний, тем самым блокируя реакцию воды со сталью бака.
Однако следует отметить, что скорость этой реакции может быть очень разной. Зависит от состава воды, ее температуры и не повреждено ли где-то защитное покрытие бака и подсоединенных к нему труб. Ускоренный износ анода чаще всего является сигналом нарушения целостности защитного покрытия бака. Защитные покрытия представляют собой барьеры, отделяющие сталь от воды. Их можно создать, например, керамической эмалью — очень эффективно, главное, чтобы в ней не образовывались полости. С другой стороны, цинковое покрытие, все еще очень часто используемое, работает таким образом, что в месте повреждения образуется слой оксида цинка с низкой реакционной способностью.
При повреждении защитного покрытия цинк окисляется и оксид цинка отделяет сталь от воды
Преимущества титанового анода по сравнению с магниевым анодом
Очень интересным решением, альтернативой магниевому аноду, является титановый анод. Главное преимущество этого типа анода в том, что он заменяется не, как с магниевым анодом, каждые 2-3 года, а каждые 10-12 лет. Столь впечатляющая разница в силе связана с тем, что титановая альтернатива основана на другом действии — здесь важен электрический потенциал, анодом которого является проводник, так что растворение самого титана практически незаметно. С другой стороны, магниевый анод почти полностью растворился после двух лет использования.
Читать дальше
Вам может быть интересно
Узнать больше
+ Показать больше
Новый и изношенный (растворенный) магниевый анод (фото Enersun)
Титановый анод (фото.Энерсун)
Гораздо более длительный срок службы титанового анода дает пользователю ряд преимуществ. Затраты на обслуживание сведены к минимуму, снижается риск истечения срока годности анода, что приводит к общему ухудшению качества воды и появлению неприятных запахов. Все, что мы получаем, это экономия времени и чувство безопасности. Стоимость титанового анода колеблется от 380 до 900 злотых. Это в несколько раз больше магниевого анода, но это одна из тех статей расходов, которые просто окупаются.
Титановый анод Enersun длиной 395 или 545 мм (рис.Энерсун)
Установка титанового анода намного проще по сравнению с магниевым анодом. Благодаря своим габаритам для укорачивания титанового анода не требуется УШМ, он совместим с различными баками. Все вышеперечисленные преимущества заставляют монтажников все чаще устанавливать титановый анод.
Editors BD
На вступительной диаграмме: Защитный эффект магниевого анода заключается в том, что ионы магния вытесняют ионы железа из раствора и предотвращают реакцию материала бака с водой
Существенные отличия анода от катода, которые вы упустили: Актуальные новости школы
РЕКЛАМА! Скачайте JAMB CBT прямо сейчас БЕСПЛАТНО!
Разница между анодом и катодом: Анод и катод — это терминология, используемая для обозначения выводов поляризованного электрического устройства. Это просто положительные и отрицательные клеммы аккумулятора. Катод представляет собой отрицательно заряженный электрод, а анод - положительно заряженный электрод.
Анод – это электрод, через который протекает ток. С другой стороны, катод — это электрод, от которого течет ток.
Вообще говоря, анод — это зажим, через который (обычный) ток поступает в устройство извне, а катод — это зажим, через который (обычный) ток течет из устройства.
Что такое анод?
Во время встречи членам Консорциума был представлен анод — тип электрода в электрическом устройстве, который обычно действует как положительно заряженный зажим.В аноде ток поступает к устройству извне, хотя при работе обоих электродов в обратной полярности порядок может не оставаться прежним.
В гальваническом элементе анодом является электрод, по которому ток течет к устройству; следовательно, это отрицательная клемма, хотя в электролитической ячейке анодом является электрод, в котором ток течет от внешнего генератора к аноду, поэтому в данном случае это положительная клемма.
Анод является источником положительного заряда в электрическом устройстве, которое притягивает отрицательный заряд или анион или действует как акцептор электронов.
Характеристики:
- Это положительно заряженный электрод.
- Анод притягивает электроны или анионы.
- Может быть источником положительного заряда или акцептором электронов.
Что такое катод?
Катод — это тип электрода в электрическом устройстве, который обычно функционирует как отрицательно заряженная клемма . В катод течет ток от прибора, а значит, электроны притекают к этому выводу извне.
Протекание катодного тока в электрической цепи по отношению к аноду может быть положительным или отрицательным.Он притягивает положительно заряженные катионы, а отрицательно заряженные анионы остаются в стороне.
В таком устройстве, как батарея, которая потребляет энергию, катод действует как отрицательный электрод, а в устройстве, таком как разрядная батарея, которая обеспечивает энергию, катод действует как положительный электрод.
Здесь следует упомянуть, что электрод – это проводник, по которому электрический ток входит или выходит из устройства. В общем, поток электронов всегда идет от анода к катоду, независимо от типа устройства и режима работы.
Характеристики:
- Отрицательно заряженный электрод.
- притягивает катионы или положительный заряд.
- Катод является источником электронов или донором электронов. Он может принимать положительный заряд.
Поскольку катод может генерировать электроны, которые обычно являются электрическими формами, совершающими реальное движение, можно сказать, что катоды генерируют заряд или что ток течет от катода к аноду. Это может сбивать с толку, потому что направление тока будет определяться тем, как движется положительный заряд.Просто помните, что каждое движение заряженных частиц представляет собой электрический ток.
Читайте также:
Различия между анодом и катодом
1. Анод и катод - это просто положительные и отрицательные клеммы аккумулятора.
2. Анод представляет собой электрод с током.
3. Катод – это электрод, от которого течет ток.
4. Катод – это ток, протекающий от электрода.Он имеет большое количество электронов.
5. В аноде ток течет к устройству извне, а в катоде ток течет из устройства, что означает, что электроны текут к этому выводу извне.
Если вам понравилась эта статья, подпишитесь на свой адрес электронной почты, чтобы получать соответствующие материалы. Спасибо.
Команда ДНС.
Присоединяйтесь к более чем 5 миллионам подписчиков сегодня!
=> ПОДПИСЫВАЙТЕСЬ НА НАС НА Instagram | FACEBOOK & TWITTER ДЛЯ ПОСЛЕДНЕГО ОБНОВЛЕНИЯ
Нравится:
Нравится Загрузка...
.


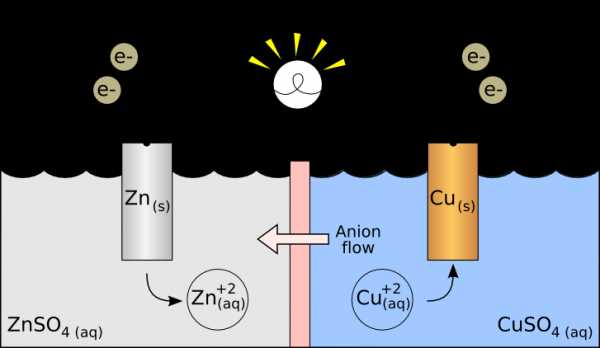











 Вызов дизайнера:
Вызов дизайнера: